| 오송첨단의료산업진흥재단 신약개발지원센터 | |
|---|---|
| Date 2019-04-09 14:32:23 |
|

센터장
오송첨단의료산업진흥재단 신약개발지원센터
tglee@kbiohealth.kr
1. 오송첨단의료복합단지(오송첨복단지)란?
오송역에서 자동차로 5분 정도를 달리면 1,131천m2(34만평)규모의 오송첨단의료복합단지(이하 ‘오송첨복단지’라 함)를 만나게 된다. 오송첨복단지는 의료산업을 차세대성장동력산업으로 육성하기 위해 조성되었다. 2000년대 초반부터 첨단복합단지의 필요성이 제기되면서, 2005년 의료산업선진화위원회가 출범되었고, 2008년 3월 「첨단의료복합단지 지정 및 지원에 관한 특별법」이 제정되었다. 이 법안에 근거하여 첨단의료복합단지 조성 계획이 발표되었고, 오송첨복단지 안에서 중추적인 역할을 하는 ‘오송첨단의료산업진흥재단(KBIOHealth, 이하 ‘오송재단’이라 함)’이 3개 중앙부처(과학기술정보통신부, 산업통상자원부, 보건복지부)와 충청북도의 참여로 2010년 12월 10일에 설립되었다.
오송첨복단지에는 의약품과 의료기기의 연구개발을 촉진 할 수 있는 다양한 물리적·제도적 환경이 조성되어 있다. 단지 내에는 기업(84개), 학교(6개), 공공기관(13개), 병원(1개) 등 산·학·연·병이 밀집되어 있어 다양한 연구 교류를 통해 시너지를 창출하고 있으며, 인근에는 식품의약품안전처, 질병관리본부, 국립보건연구원 등이 위치한 보건의료행정타운과 엘지화학, 메디톡스 등 다수의 의약품 생산시설이 마주하고 있어 R&D, 인허가, 생산이 결합된 바이오산업의 최적지를 형성하고 있다(그림 1).
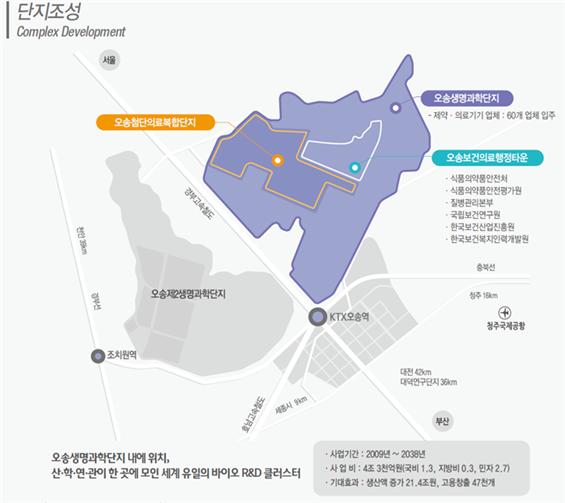
그림 1. 오송생명과학단지 내에 위치한 오송첨단의료복합단지
또한 제도적으로도 「첨단의료복합단지 지정 및 지원에 관한 특별법 시행규칙」을 통해 신약 및 의료기기의 임상연구를 용이하게 할 수 있도록 다양한 특례들을 보장하고 있다. 첨복단지 내의 의료기관에서는 의료연구개발 목적이라면 외국 의사도 출신국 면허를 가지고 의료행위를 할 수 있으며, 복지부장관이 공익성 등을 인정한 경우 의료연구개발에 필요한 임상연구 비용을 환자 또는 국민건강보험공단이 부담하도록 할 수 있다.
2. 오송첨단의료산업진흥재단(KBIOHealth) 소개
오송첨복단지 내에 소재한 오송첨단의료산업진흥재단(https://www.kbiohealth.kr)은 바이오의약품과 의료기기 연구를 지원하는 핵심기관으로서 신약개발지원센터, 첨단의료기기개발지원센터, 실험동물센터, 바이오의약생산센터로 구성되어 있다(그림 2). 총사업비 1,905억원(건축비 1,079억원, 장비비 826억원)이 투입되어 2013년 11월에 건물(부지 77,978m2, 건축연면적 45,413m2)이 완공되었고, 현재 269명(정원 410명)이 근무하고 있다. 대구에도 오송첨복단지와 비슷한 규모로 대구경북첨복단지가 조성되어 있으며, 대구 신약개발지원센터에서는 화합물신약 연구개발을, 오송 신약개발지원센터는 바이오신약 연구개발을 지원하고 있다. 오송재단은 설립 초기 과학기술정보통신부, 산업통상자원부, 보건복지부 3개 중앙부처를 주무관청으로 운영되었으나, 2018년부터 복지부산하 기타공공기관으로 일원화되어 운영되고 있다. 신약개발지원센터는 오송첨복단지 내에 소재한 기업 뿐 아니라 국내에서 바이오신약을 연구하고 있는 모든 연구자들을 지원하고 있다.
그림 2. 오송첨단의료산업진흥재단 전경. A: 신약개발지원센터, B: 첨단의료기기개발지원센터, C: 실험동물센터(신약센터 뒤에 위치함) D: 바이오의약생산센터
3. 바이오의약산업의 특성과 신약개발을 위한 국내 기술 인프라의 필요성
전 세계 처방의약품시장은 2018년 8,300억 달러에서 연평균 6.4%로 성장하여 2024년에는 1.2조 달러를 형성할 것으로 전망되고 있다. 또한 2017년 2,020달러 규모였던 바이오의약품 시장은 오는 2024년 까지 3,803달러로 성장하여 전체 의약품시장에서 31% 차지할 것으로 전망 되고 있으며, 특히 상위 100개 의약품 중 52%를 바이오의약품이 차지할 것으로 예상되고 있다.
현재 신약 1개를 개발하기 위해서는 13.5년의 긴 시간과 2조 원(직접 비용 3,000억 원 및 기타 모든 간접비용 포함) 가량의 천문학적인 비용이 요구된다. 하나의 신약이 시장에 출시되기까지는 다양한 개발 과정을 통해 유효성과 안정성을 검증해야한다. 먼저 약물이 작용하는 작용점(drug target)을 찾아 검증을 거친 후, 이 작용점을 조절하는 초기물질(Hit)부터 선도물질(Lead)을 발굴하는 과정을 거쳐 최종적으로 후보물질(Candidate)을 발굴하고 제조하여야한다. 신약 후보물질은 동물에서의 비임상 독성시험을 통해 안전성이 확보되고, 임상1/2/3상을 통해 사람에서의 안전성과 유효성이 입증된 후 식약처 허가를 받아야만 신약으로서 의약품 시장에 출시될 수 있다. 임상1상에서 허가까지 성공률은 보통 10~30% 정도로, 신약개발은 대표적인 ‘고위험 고수익(high-risk high-return)’ 투자분야라고 할 수 있다.
그러면 국내 의약품산업을 차세대 성장동력으로 육성하기 위해서는 무엇이 필요한가? 이에 대한 논의는 오송첨복단지 조성 때부터 계속되어왔다. 신약개발을 위해서는 기초연구부터 임상연구에 이르기까지 매우 다양한 기술과 우수한 역량을 지닌 연구자들이 필요하다. 또한 이는 글로벌기업과 경쟁할 수 있는 수준을 갖추어야 한다. 예를 들어, 대학교와 연구소로부터 나온 초기연구 결과물을 신약개발로 발전시키려면 충분한 연구개발비 뿐만 아니라, 경쟁력 있는 신약개발을 지원할 수 있는 글로벌 수준의 인프라가 필요하다. 미국, 유럽과 같은 제약 선진 국가의 경우 다국적 제약기업의 지원뿐만 아니라, 실험을 대행해주는 다양한 전문적인 CRO(Contract Research Organizatoin)가 잘 발달되어 효율적인 신약개발이 가능하지만, 국내의 경우 역량이 많이 부족한 상황이다.
4. 바이오신약개발을 위한 오송 신약개발지원센터의 역할
신약개발지원센터는 이와 같은 문제를 해결하고자 설립되었다. 신약개발지원센터에서는 항체치료제, 단백질치료제, 유전자치료제 등 바이오신약 개발을 위해 필요한 주요 기반기술을 구축하여 산·학·연의 연구자들이 우수한 신약개발후보물질을 신속하게 발굴하여 임상단계로 진입할 수 있도록 지원하고 있다(그림 3). 예를 들어 연구자가 암을 유발하는 단백질을 발굴한 후 이를 억제할 수 있는 항체로 항암신약을 개발하고자 한다면, 신약개발지원센터를 통해 항체를 찾는 과정부터 대량 배양 정제, 세포주 개발 그리고 분석까지의 전 과정을 지원 받을 수 있다. 일반적으로 알려진 CRO와의 차이점을 든다면, 바이오신약개발 전반에 대해 컨설팅부터 연구개발 지원까지 신약개발의 파트너로서 성공을 위해 공동의 노력을 기울인다는 점이다. 이러한 신약개발 통합 지원 시스템은 연구개발에 필요한 전반적인 사항을 미리 점검하고 지원함으로써 신약개발 연구 경험이 부족한 기초연구자와 벤처창업자에게 특히 많은 도움이 되고 있다.
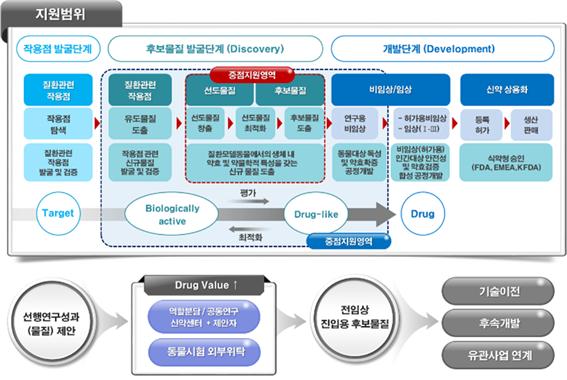
그림 3. 신약개발과정 및 오송 신약개발지원센터의 중점지원영역
신약개발지원센터는 국가 및 민간과제의 공동연구나 위탁연구, 단순 장비 활용지원까지 다양한 형태의 신약개발 지원을 제공하고 있다(그림 4).
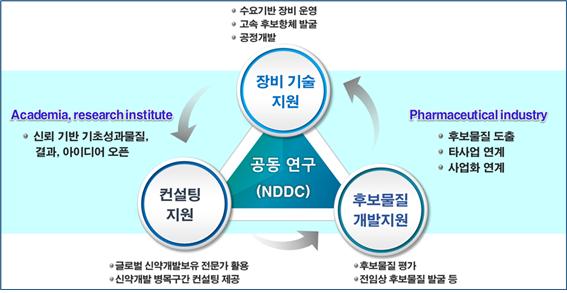
그림 4. 신약개발지원센터의 지원방식
오송재단에서는 매년 과학기술정보통신부 ‘기반기술구축사업 최적화지원과제’와 ‘충청북도 가치창출사업’ 공모를 진행하고 있다. ‘기반기술구축사업 최적화기술지원과제’는 신약개발지원센터에 구축된 기반기술을 활용하여 산·학·연을 지원하는 과제로 매년 11월 경 신규과제를 공모한다. 본 과제는 비영리 연구기관이나 영세한 국내 중·소벤처기업을 대상으로 유망성이 있으나 산업화 역량이 부족하여 사장의 위험성이 있는 신약개발 기초 연구성과물의 연구공백을 지원하여 다음 단계로 진입할 수 있도록 조력하는 것을 목표로 한다. 최대 2년 동안 연 5천만 원~2.5억 원을 지원하며, 단순히 연구개발비를 지원하는 것이 아닌 신약개발지원센터에서 직접 연구를 수행하고 도출된 연구결과물을 공유하여 대형 국가연구개발사업이나 기술이전 단계에 진입할 수 있도록 포괄적으로 지원하고 있다. 이와 별개로 충청북도에 위치한 기관은 ‘충청북도 첨단의료기술 가치창출 사업’에 지원할 수 있다(매년 10월 경 공고, 2억 내외). 또한 올해부터는 다부처(보건복지부, 과학기술정보통신부, 산업통상자원부) 사업이 진행될 예정이다.
이외에도 바이오의료개발기술사업 등 정부부처 사업에 세부나 위탁과제 형태로 참여하여 공동연구를 지원하거나, 항체발굴, 단백질 특성분석, 세포주 개발 및 생산, PK 분석, 바이오의약제형 개발 등과 관련된 다양한 기술용역과제를 지원하고 있다. 또한 중·소 벤처기업이나 학교에서 구축하기 힘든 고가 장비를 센터 내에 집약하여 저렴한 비용으로 장비활용서비스를 제공하고 있다.
신약개발센터에서는 2018년까지 후보물질 발굴과제 46건, 기반기술개발지원과제 43건, 기술서비스지원 169건, 인프라활용서비스지원 678건등 총 162기관을 대상으로 936건의 신약연구개발을 지원하였다. 이 중 다수의 성과물이 국내외로 기술이전되었으며, 후속 연구개발이 활발히 진행되고 있다. 또한 2015년부터 3년간 글로벌첨단바이오의약품사업 코디네이팅센터(CoGIB http://www.cogib.kr) 운영을 통해 유전자치료제와 줄기세포치료제 개발 기업의 비연구분야를 지원하며 다수 기업의 임상 진입을 지원하였다.
신약개발지원센터는 매년 2회 부트캠프를 통해 서울, 판교, 대전 등에서 센터의 보유기술을 소개함으로써 지원기관 확대를 위한 노력을 계속하고 있다. 2012년부터 현재까지 매년 10월경 ‘Osong BioExcellence& BioSymposium’을 개최하여 바이오의약의 연구, 개발, 허가에 이르는 과정에 대한 정보를 공유하는 자리를 마련하고 있다. 2018년에는 nanobody분야와 단백질 공학 대가인 S. Muyldermans박사와 A. Skerra 박사를 초청하여 나노형태의 소형화된 항체진단치료제 개발과 단백질 PASylation 기술에 대한 경험을 공유하였으며, 국내 유망 벤처 제약 기업의 신약개발 파이프라인 소개를 통해 후발 기업들에게 다양한 정보를 제공하였다.
5. 오송 신약개발지원센터 조직과 보유기술
신약개발지원센터는 재단 건물이 완공된 2013년 11월부터 본격적으로 우수인력 채용과 장비 등 핵심시설구축을 시작하였다. 2014년 중반부터는 과학기술정보통신부의 오송 신약개발지원센터 R&D 지원사업을 통해 바이오신약개발 지원에 필요한 핵심 기반기술을 지속적으로 갖춰 가고 있다. 신약개발지원센터는 현재 5부 10팀으로 구성되어 있으며, 총 91명의 연구진이 근무하고 있다. 신약개발지원센터의 조직은 센터 운영과 연구기획을 담당하는 신약연구기획지원부, 항체의약품팀과 단백질의약품 그리고 첨단의약품팀으로 구성된 신약개발최적화지원부, 약리약효평가팀과 독성PK지원팀으로 구성된 신약약효평가지원부, 셀라인배지개발팀과 생산공정기술팀, 제형기술팀으로 구성된 신약개발프로세스지원부 마지막으로 바이오의약분석팀이 소속된 융합기술지원부로 구성되어있다. 신약개발지원센터는 각 팀명에서 알 수 있듯이 항체, 단백질, 유전자치료제등 바이오신약 개발 단계의 비임상 연구 전반을 지원하기 위한 조직으로 구성되어 있으며, 그에 필요한 다양한 기반기술을 갖춰 놓고 있다.
신약개발최적화지원부 항체의약품팀은 강원대 연구진과 함께 인간 합성 Fab 및 scFv 파아지라이브러리를 구축하였고, 현재 colony picker등의 자동화 장비를 활용한 phage panning을 통해 초기 항체 물질발굴을 지원하고 있다. 또한 cell panning, immune phage display 라이브러리 등을 활용한 항체발굴 기술도 갖추어 놓고 있으며, 이외에 Discovery studio를 활용하여 신약개발을 위한 in silico 모델분석도 활발히 수행하고 있다. 단백질의약품팀은 국민대 연구진과 항체의 Fc를 변형시켜 혈중 반감기가 극대화된 항체 발굴에 성공하였다. 본 기술은 현재 해당 분야 최고기술을 지닌 Xencor사의 기술보다도 우수한 반감기와 세포사멸활성(CDC) 효과가 있는 것으로 나타났으며, 국내 바이오벤처기업과 일부 품목에 한정하여 기술실시계약을 체결하였다. 본 팀은 동물 항체를 인간 항체로 변경시키는 humanization기술도 보유하고 있으며, 이를 통해 다수 국책연구과제를 지원하고 있다. 또한 Octet, Biacore장비를 활용하여 항체와 표적단백질 또는 펩타이드간의 결합력 평가를 지원하고 있다. 첨단의약품팀은 유전자치료제 개발 지원을 위한 바이러스 벡터 생산 및 정제공정기술을 갖추고 연구용 또는 비임상 시험용 바이러스 생산을 지원하고 있다. 최근에는 CAR-T, CAR-NK 치료제 개발 지원 플랫폼기술을 갖추고 in vitro, in vivo 효능평가를 지원하고 있다.
신약약효평가지원부의 약효평가지원팀은 항체에 의한 세포사멸 활성(ADCC, CDC)을 세포주 혹은 사람 말초혈액면역세포(PBMC)를 사용한 평가와 FACS 장비를 활용한 세포 특성 분석, MSD(Meso Scale Discovery)를 활용한 다양한 세포 증식 및 활성인자 분석을 지원하고 있다. 특히, 바이오의약품은 인체에 투여 시 면역원성을 유발하여 약효를 감소시키거나 자가면역질환과 같은 심각한 부작용을 유발할 수 있어, 개발 과정에 면역원성 유발 가능성을 사전에 예측하여 제거하는 것이 필요하다. 바이오의약품의 면역원성 평가를 위해 in silico 면역원성 평가법과 사람 PBMC를 이용한 in vitro 면역원성 평가법을 구축하였으며, 면역원성 유발 가능성을 조기에 예측하여 제거함으로써 신약개발 성공률을 높일 수 있도록 지원하고 있다. 독성PK지원팀은 세포 및 일반독성시험, 생체시료 내 약물농도분석과 PK/PD분석, 계량약물학적 분석과 모델링을 통해 임상투여용량 예측 등을 지원하고 있다. 또한 세포 및 유전자치료제의 생체분포 평가를 위한 정량적 PCR 분석 기술을 확립하여 지원하고 있다.
프로세스지원부 셀라인배지개발지원팀에서는 ClonePix를 활용하여 고성장, 고발현의 재조합단백질 생산 세포주를 개발하고 있고, Cell Metrix장비를 이용하여 단일세포 유래입증 및 선별을 하고 있다. 또한 현재 6개 다국적배지 제조사들과 업무협약을 통해 기본배양배지 100여종, 유가식배양배지 30종을 적용해서 생산 세포주별 최적화된 배지 선별을 지원하고 있다. 그리고 5 L 규모의 플라스크 일시발현 시스템과 bioreactor 배양을 통해 후보물질 특성을 연구에 필요한 비임상 시료 생산을 지원하고 있다. 생산공정기술지원팀에서는 설계기반 품질고도화(QbD)를 통해 항체, 재조합 단백질, 세포치료제 생산을 위한 제조공정 전략을 수립하고 있으며, 배양공정과 정제공정에 모두 적용하여 대량정제공정 파라미터를 확립하고 있다. 배양공정 확립과 비임상시료를 생산하기 위해 마이크로바이오리액터 Ambr15, Biostat Q plus(1L), Biostat B(3~10L), Celligen 310(1~10L), Biostat CultiBag(50L), Celligen BLU(10~40L), ATF-4, -6 시스템, 심층여과시스템(depth filtration)을 갖추고 있다. 정제공정을 위해 AKTA Avant와 Pilot, Sartoflow advanced Cogent M1 TFF, FlexAct System을 활용하고 있다. 또한 제형개발지원팀에서는 바이오신약의 stress, stability indication assay를 통해 바이오의약품의 불안정화의 주요인자를 발굴하여 바이오신약을 안정화 시킬 수 있는 선도제형 연구개발을 지원하고 있다. 그리고 DOE(Design of Experiment)를 통한 동결건조 사이클 최적화를 통해 동결건조제형개발을 지원하고 있다.
마지막으로 융합기술지원부 바이오의약분석팀에서는 단백질의약 분석을 체계적으로 지원하고 있다. ESI-MS 질량분석기를 이용한 단백질 분자량 분석, chromophore RapiFluor를 이용한 고감도 glycan profiling 분석을 지원한다. Maurice 모세관전기영동장치(CE)를 이용한 단백질의 charge variant, MW, impurity 분석과 SEC(Size Exclusion Chromatograph)을 이용한 단백질 aggregate 분석을 지원한다. 또한 질량 분석기를 이용하여 ADC(Antibody Drug Conjugate), 약물학적 동태, 단백질의 PTM(post translational modification)을 분석하고, 펩타이드 분석을 통해 단백질 동정, 바이오마커 발굴, PK 분석 등을 지원하고 있다. 최근에는 기반기술 과제를 통해 특정 RTK(receptor tyrosine kinase)에 작용하는 억제제 처리에 따른 세포 내 다양한 RTK의 발현량과 활성을 동시에 분석하는 RTK 통합분석 시스템을 구축했다. 특히, HDX(hydrogen deuterium exchange)-MS를 이용한 epitope mapping기술은 항체와 결합하는 표적 단백질의 결합 부위 동정 및 바이오시밀러의 유사성 분석 등 활용도가 넓어 최근 연구자들의 수요가 점점 증가하고 있는 기술이다. 보다 상세한 기술 및 지원서비스는 홈페이지에서 확인할 수 있다. (https://www.kbiohealth.kr/content/view.do?menuKey=40&contentKey=6 )
6. 오송 신약개발지원센터의 앞으로의 발전방향
오송 신약개발지원센터는 바이오의약 연구에 필요한 기술 인프라를 집약한 센터이다. 센터가 발전하기 위해서는 무엇보다 구축된 기술이 우수해야 한다. 그래야 연구·개발자들이 바이오신약 연구를 위해 많이 활용할 수 있을 것이다. 이를 위해 신약개발지원센터는 글로벌 경쟁력이 있으며, 국내 중소·벤처기업에서 구축하기 어려운 기술을 지속적으로 구축해 나갈 것이다. 혈액 내에서 항체의 혈중반감기를 증가시킨 기술, HDX를 이용한 epitope mapping기술, 면역원성 측정기술 등은 센터 보유 기술 중 글로벌 경쟁력을 지닌 기술들이다. 또한 바이오의약 제형연구는 국내 개별 중소·벤처기업에서 구축하기 힘든 기술로 매년 수요가 지속적으로 증가하고 있는 기술이다. 이와 같이, 센터는 앞으로도 계속하여 연구자들의 수요에 맞추어서 기술을 구축하고 지원할 것이다. 또한 이에 맞춰 센터 보유 기술들을 홍보하고 교육하는 과정도 점차적으로 확대해 나갈 것이다.
현재 신약개발지원센터는 자립화를 위해 노력하고 있는데, 센터에서 제공하는 기술지원을 통해 확보한 재원만으로 센터를 발전시키고 경쟁력 있는 장비를 갖추어 나가기에는 매우 부족한 실정이다. 비록 시간이 걸리겠지만, 신약개발지원센터와의 공동연구를 통해 개발된 신약 물질이나 바이오 기반기술이 기술적 가치를 인정받아 기술이전 등을 통해 신약개발지원센터로 재투자된다면 자립화를 달성하는 데 큰 기여를 할 것이라 생각한다. 바이오신약개발을 위해 필요한 핵심 기술을 신약개발지원센터 연구원의 역량만으로 모두 갖출 수 없다. 우수한 국내외 연구진들과 협력해야 보다 나은 수준의 기술을 구축할 수 있다. 그렇기 때문에 센터는 국내 대학교나 연구소 등에서 바이오의약품 개발을 위해 각고의 노력을 다하고 있는 연구진과 지속적으로 협력을 확대해 나가고자 한다.
센터가 역점을 두어야 할 또 다른 분야는 기초연구와 임상의 연결이다. 중개연구 또는 translational study 라고 하는 이 분야에서 필요로 하는 역량을 점진적으로 갖추어 나가 신약개발지원센터가 의료산업 혁신성장의 초석이 되기를 바란다.
결론적으로, 신약개발지원센터의 역할은 국내의 수많은 초기 연구결과물들이 후속 연구로 이어져서 글로벌 바이오신약을 개발할 수 있도록 기여하는 촉매 역할을 하는 것이다. 그 결과 바이오의약산업이 국가의 미래를 담당할 핵심성장동력으로 자리 잡게 된다면, 이것이 바로 센터가 추구해야 할 최우선 공적 역할이 될 것이다. 성공적인 지원과 환류를 통해 신약개발지원센터의 자생력을 갖추어 안정적인 신약개발지원 환경이 조성될 수 있도록 지속적인 관심과 충고를 부탁드린다.
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update 

