| COVID-19의 진단 기술 및 전망 | |
|---|---|
| Date 2020-10-21 00:07:53 |
|

대표이사
Apteasy MJ inc.
lok103@hanmail.net
1. 서론
인류가 발전하기 시작하면서부터 다양한 미생물을 유용하게 이용하기도 하고 다양한 미생물에 의해 인류가 위험한 경험도 다수 발생하고 있다. 과거에 흑사병, 괴질 등의 질환은 많은 생명을 가족에게서 빼앗아가기도 하였다. 항생제의 발달로 인해 이러한 미생물에 의한 감염성 질환에서 벗어나기 시작한 현 인류는 2000년대 이후 새로운 위험에 직면하고 있다.
이들은 바이러스로 불리우며, 다른 유기체의 살아 있는 세포 안에서만 생명 활동을 하는 전염성 감염원이라 생물과 무생물의 중간적 존재를 의미 한다 [1].
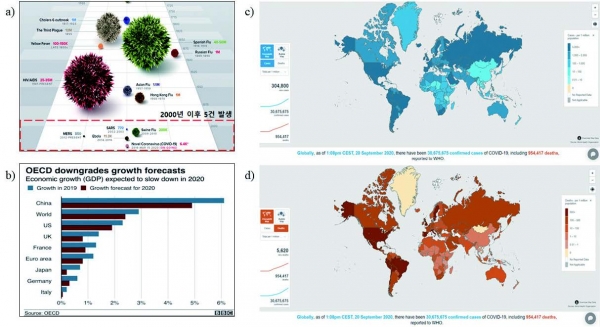
그림 1. a) 근대 이후 바이러스 발생 현황 및 사망자 수 (W H O 통계), b) OECD 국가별 COVID-19 발생 전후 경제 성장률 예측 표 (OECD 자료),
c) COVID-19 발생 현황 (WHO, 20.09.21), d) COVID-19 발생 사망자 현황 (WHO, 20.09.21) [2].
현 인류는 2000년대 이후 5번의 신규 바이러스에 노출로 인한 인명, 경제적, 사회적 손실을 일으켰다. SARS (2002), Swine Flu (2009), MERS (2012), Ebola (2014), COVID-19 (2019) 이 그것이다. 이 외에도 지카 바이러스, 조류인플루엔자 등의 발생으로 인해 세계적인 사회, 경제적 손실이 발생하였으며 세계은행 추산 금액만 916조에 이른다고 보고되었다.
그리고, 무엇보다 현재 우리 인류는 COVID-19의 범유행 상황을 맞이하고 있으며 종식 불확실성에서 마스크, 접촉제한, 등교 제한 등의 불편함을 겪고 있다. 이로 인해 전세계 다수의 기업과 자영업자와 같은 경제활동체의 피해가 지속되고 있으며 앞으로 더 심각해질 것으로 예측되고 있다 (그림 1b). 그리고 그 피해 금액이 아시아 은행의 예측으로는 1경 6천억 원이라는 천문학적인 수치가 될 것으로 보고되고 있다.
현재 COVID-19의 WHO에서 보고된 환자 발생 수는 3,000만 명을 넘겼으며 그림 1c에서 확인할 수 있듯이 지속적인 증가 추세선을 보여주고 있다는 점이 그리 낙관적인 점은 아닐 것으로 보인다. 또한, 사망자 역시 WHO에서 보고된 수가 95만 명을 넘었으며 지속적으로 환자가 발생한다는 점을 고려할 때 사망자의 수는 100만 명을 넘길 것으로 예측되고 있다. 대략 국내 광역시 인구수가 100만 명 이상임을 고려할 때 해당 숫자는 가히 짐작하기 어렵다.
다만, 다행인 점은 감염 추이나 감염성을 볼 때 더 많은 숫자의 감염자 및 감염으로 인한 사망자가 발생할 수도 있었 으나 국가별로 방역 시스템 및 진단 시스템의 강화로 인해 즉각적인 검사 및 격리, 치료 조치가 이뤄져 더 큰 확산을 방 지하고 있다는 점이다.
2. COVID-19의 진단에 이용되는 주요 특징
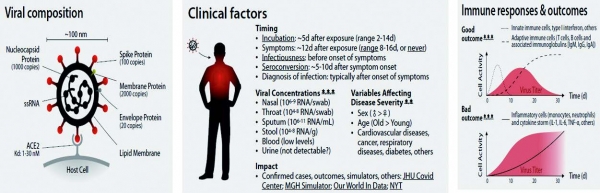
그림 2에서 처럼 COVID-19 진단을 위한 검출 대상 (Target) 은 바이러스 표면의 단백질인 spike protein, 바이러스를 불활성 시킨 후 측정할 수 있는 nucleocapsid protein, 증폭이 가능한 ssRNA, 감염 후 면역반응에 의해 측정할 수 있는 IgG, IgM으로 나눌 수 있다.
또한, 시료 채취도 진단 플랫폼에서는 중요한 요소이기 때문에 분자진단의 경우 비교적 접근이 쉽고 시료의 양이 많은 비강, 기도 등에서 이뤄지고 있으며 면역반응 후 발생된 항체의 경우에는 혈액을 통해서 진행되고 있다. 가장 많은 시료를 포함하고 있는 객담 (sputum)의 경우는 시료를 분리 정제하는 데 걸리는 시간이 다른 시료에 비해 길기 때문에 잘 사용이 되지 않고 있다 [3].
그림 2. COVID-19의 진단을 위한 특징
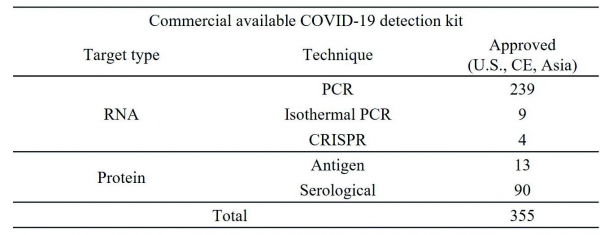
위 특징을 기반으로 사용 승인이 된 제품은 전 세계적으로 355개이며 현장에서 방역을 위해 사용 되고 있다 (표 1).
이렇게 짧은 시간 내에 많은 제품이 개발되고 현장에서 바로 사용이 되었던 경우는 이례적이라고 할 수 있다. 그만큼 COVID-19이 전 인류의 생존을 위협하고 있으며, 이를 막기 위해서는 방역의 기본인 진단 시스템을 빠르게 구축하기위해서라고 보여 진다. COVID-19의 특성상 1개의 바이러스에만 노출이 된다 하더라도 감염성을 가질 수 있으므로, 극소량도 민감하게 진단해낼 수 있는 PCR 기반 기술이 전체 개발된 기술의 대략 71%를 차지하고 있으며, 또한 보다 신속한 현장 진단을 위해 감염 후 발생하는 면역 산물을 측정하는 방법 및 직접적 감염원인 COVID-19을 측정하는 방법 등이 나머지 29%를 차지하고 있다.
표 1. 상용화된 COVID-19 검출 Kit의 검체별, 기술별 통계
Coronavirus Test Tracker: Commercially Available COVID-19 Diagno stic Tests 분석 [4]
3. Target type에 따른 COVID-19 주요 진단 기술
3.1. RNA 기반 진단 기술
그림 2에서 확인한 것처럼 COVID-19는 ssRNA 형태의 바이러스로 알려져 있다. 따라서 RNA를 cDNA 로 치환 (reverse transcription) 한 후 감염 여부를 확인하는 PCR 기반 기술이 주를 이루고 있으며, 이를 바탕으로 현재 개발되어진 PCR 법의 대표적인 방법으로는 quantitative reverse transcription PCR (qRT-PCR) 과 isothermal PCR로 구분할 수 있다. 또한, 최근에는 CRISPR/Cas를 접목한 방법들도 제안되고 있다.
3.1.1. Quantitative reverse transcription PCR (qRT-PCR)
qRT-PCR 은 기술적으로는 일반적인 PCR 방법과 동일하나, ssRNA 를 cDNA 로 치환해 주는 과정 (reverse transcription)이 추가로 들어가며 형광 측정 장비를 기반으로 형광 염색 혹은 형광 probe를 이용하여 증폭 정도를 실시간으로 분석할 수 있다. 이를 통해 높은 민감도로 COVID-19 감염 여부를 정량적으로 진단해 낼 수 있다. 전 세계적으로 대략 239개의 상용화 제품 (전체 상용화 제품 중 67% 점유율)에 사용되는 기술이다. 현재 COVID-19를 진단함에 있어 표준 방법으로 사용되고 있다.
3.1.2. Isothermal PCR (등온 PCR)
Isothermal PCR 기술은 등온 (항온)에서 유전자 증폭을 야기시키는 기술로 기존의 PCR 방법과는 상이하게 온도의 변화 구간이 없어 비교적 증폭이 빠른 시간 내에 완료되는 것이 특징이다.
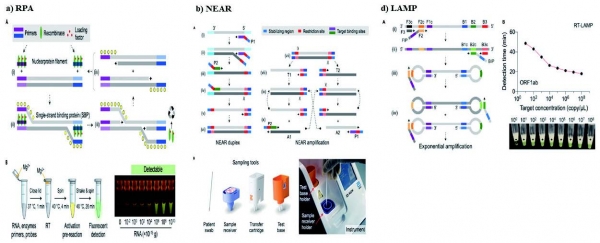
그림 3. a) RPA 기반 COVID-19 진단 기술, b) NEAR 기반 COVID-19 진단 기술, c) L AMP 기반 COVID-19 진단 기술
등온 PCR의 경우는 사용되는 효소, 검체, primer 형태, denaturation method 등에 따라 다양한 이름으로 개발되어져 있으며 대표적인 방법론으로는 LAMP (Loopmediated Isothermal amplification), NASBA (Nucleic Acid Sequence Based Amplification), SDA (Strand Displacement Amplification), HDA (Helicase Dependent Amplification), NEAR (NIcking enzyme amplification reaction), RPA (Recombinase polymerase amplification) 등이 있다.
그림 3에서 확인할 수 있듯이 위의 다양한 기반의 등온 PCR 중 COVID-19 진단 기술로는 LAMP, NEAR, RPA 같은 방법들이 개발되어 있다 [5].
3.1.3. CRISPR/Cas 기반 기술
현재 COVID-19 진단에 쓰이고 있는 qRT-PCR 방법은 장비적인 제약 및 상대적으로 긴 반응 시간이라는 문제점을 가지고 있기 때문에, 등온 PCR 뿐만 아니라 다른 방법들이 제안되어 왔다. 그 중에서도 CRISPR/Cas 시스템이 최근 각광을 받고 있는 상황이다 (references 추가).
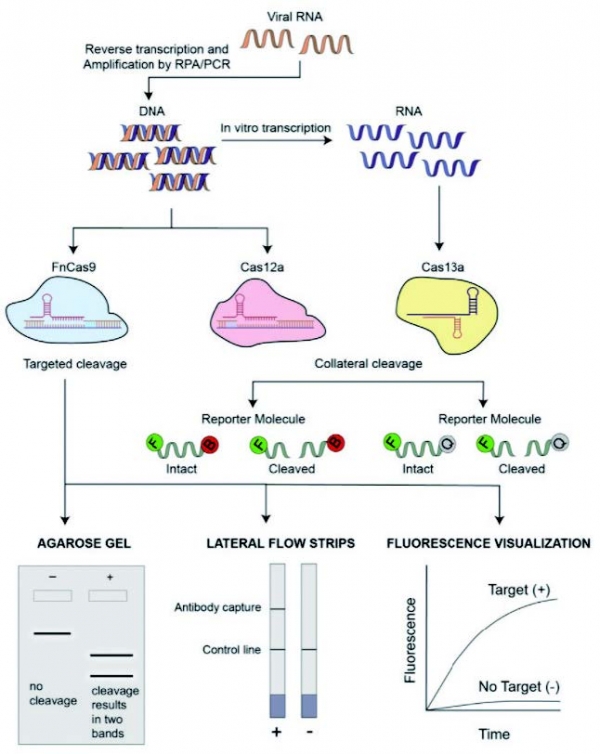
CRISPR/Cas를 이용한 진단 기술의 전체 과정을 살펴 보면, 크게 3가지 부분으로 나뉠 수 있다. 첫 번째는 초기 증폭 과정이다. 이 과정에서 viral RNA를 cDNA 로 전환하여 전형적인 PCR 및 등온 PCR을 진행하여 증폭된 DNA 산물을 얻는다. 이렇게 얻어진 DNA 산물을 그대로 사용하거나 추가로 T7 RNA polymerase 를 이용하여 한 번 더 증폭하는 과정을 통해 RNA 산물을 사용하기도 한다. 두 번째는 CRISPR/Cas를 통한 반응 과정이다. 이 부분에서는 dsDNA를 절단하는 FnCas9, dsDNA를 절단한 후 비특이적으로 ssDNA를 절단하는 활성을 나타내는 Cas12a, ssRNA 에 결합한 후 비 특이적으로 ssRNA를 절단하는 활성을 나타내는 Cas13a 가 사용된다. 세 번째는 신호 검출 과정이다. FnCas9 을 사용한 경우 절단된 산물을 아가로즈젤로 확인을 할 수 있고, Cas12a 및 Cas13a 와 같이 비특이적으로 ssDNA 나 ssRNA를 절단하는 경우 F/Q 가 달린 reporter probe 로부터 형광세기의 변화를 통해 진단하거나 lateral flow strip 에 반응할 수 있는 reporter probe를 통해 진단할 수 있다 [6].
그림 4. CRISPR/Cas 시스템을 도입한 COVID-19 진단 과정의 전체 모식도
3.2. 단백질 기반 진단 기술
단백질 기반 측정 기술은 그림 2에서처럼 항원의 단백질을 직접적으로 측정하는 방식과 간접적으로 감염 후 면역체 계의 산물인 IgG, IgM을 측정하는 방식으로 크게 구분 할 수 있다. 항원을 직접 측정하는 기술의 경우에는 현재 감염 여부를 측정할 수 있다는 장점이 있는 반면에 검출 감도가 충분하지 못해 위음성 발생으로 인한 잠재 감염자 노출 위험이 있다. 간적접인 방법인 면역 산물인 IgG 및 IgM을 측정하는 방법은 감염 후 2~3일의 시간이 흐른 후에 검출이 가능 하다는 점이 위험 부담일 수 있으나 생성 양이 많아 비교적 빠른 시간 내에 검출이 가능하다는 장점이 있다.
대표적인 방법론으로는 전통적인 항원 항체 검출 기술인 ELISA 방법 및 LFA 기법이 주로 사용되며 microarray, western blots, immunofluorescece microscopy 같은 방법도 병행되어 사용되고 있다.
단백질 기반 기술의 핵심은 항원 항체 반응에 기초한다. 특정 항원은 특정 항체와 결합한다는 것을 이용하여 측정을 진행한다.
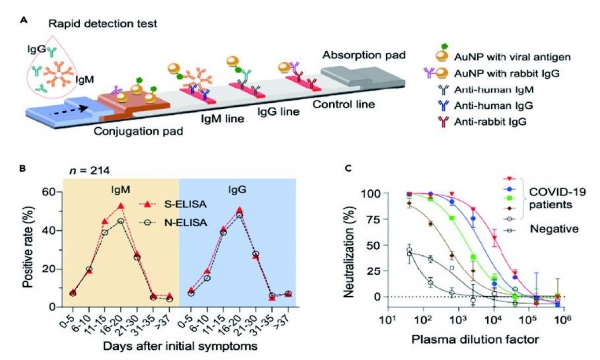
그림 5. A) LFA system, B) COVID-19 검출 결과, C) 혈장 내 COVID-19 항체 생성도
3.2.1. LFA (Lateral flow assay)기반 측정 기술
LFA 기술은 임신진단 Kit와 같이 면역화학반응을 통한 신속한 검출에 사용되는 기술로 항원과 항체 조합을 기반으로 하여 특정 항원에 특정 항체가 결합하는 특성을 이용하여 검출하는 기술이다. 검출 대상에 따라 항원을 직접적으로 검사하는 방법이 있을 수 있으며 해당 항원에 대한 면역반응의 산물인 항체를 검사하는 방법을 이용할 수도 있다. 두 방법의 경우는 상황 및 목적에 따라 다를 수 있다.
항원을 직접적으로 검사하는 경우 현재의 감염 여부를 확인함에 유용하나 항원이 특정 농도 이상 (104 이상) 존재하지 않는 경우에는 검출이 되지 않을 수도 있다. 항원에 대한 항체를 검사하는 경우 현재의 감염원의 상태를 확정적으로 표현하기는 어려울 수 있으나 검체의 양이 많아 검출 감도에 대한 여부를 고려하지 않아도 되며 감염 이력을 확인할 수 있다.
현재 COVID-19의 경우에도 항원, 항체 검사 2가지 형태의 LFA 기술이 개발되어 있으나 주로 항체 검사를 이용하고 있다. 이유는 위에 언급하였듯이 감염 초기에 시행하는 경우 항원 검사의 경우에는 검출이 되지 않는 경우가 발생하기 때문이다.
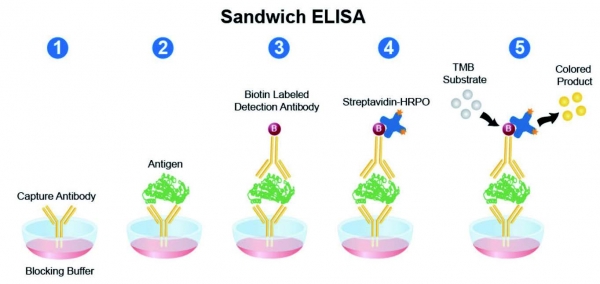
3.2.2. ELISA (Enzyme-Linked Immunosorbent Assay) 기반 측정 기술
ELISA는 기술적 특징은 LFA 와 유사하게 항원항체 결합을 기반으로 하여 구동되며 LFA 처럼 단독 검사를 대상으로 하기보다는 대량의 검사에 유용하게 사용되는 검사법이다. Microplate 의 capacity에 따라 달라지긴 하지만 일반적으로 96개의 검체 검사를 동시에 수행할 수 있는 장점이 있다. 또한, 효소반응을 통해 기질을 소모하여 검출 신호의 강도를 강하게 만들어 줌으로 인해 신호 증폭 효과도 동반하는 기술이다. COVID-19 를 검사함에 있어서는 대다수 혈청에 있는 COVID-19 항체 검사에 이용하고 있다.
그림 6. ELISA 기술 모식도 [7]
4. 결론
COVID-19 의 발생으로 인해 국내의 다수의 진단 기업들은 세계적으로 기술력을 인정받았다. 또한, 세계는 힘을 합하여 해당 질환을 이겨내기 위해 다양한 제품을 시장에 제공하고 있다. 그리고, 치료제 및 백신의 개발을 위해 각 국가 및 기업은 천문학적인 자금을 지원하고 투자하고 있다. 시기를 특정 지을 수는 없지만 결실을 볼 수 있을 것으로 예측된다.
염려되는 것은 유래 없는 감염병인 COVID-19 로 인해 기존의 일상이 흔들리고 건강이 위협받고 있으며 무엇보다 어 려운 부분은 이 질병이 언제, 어떻게 종식될 수 있을지 가늠할 수 없는 불확실성이 가장 큰 문제라고 생각된다. 현재도 초기 발생형태가 아닌 변종의 COVID-19 바이러스는 발생이 되고 있으며 기존의 COVID-19 발병 환자가 재감염되는 상황도 보고되고 있다. 따라서, 진단 관련 기업들은 끊임없이 정확성, 신속성, 간편성을 겸비한 진단 시스템을 확고히 구축해 나가야 할 것이다.
또한, 질환으로 인한 건강의 위험만이 문제가 아니라 이로 인해 발생된 가계별, 기업, 국가의 경제적 위기, 삶의 질의 하락은 더 심각하게 인식될 것이다. 이런 측면에서 우리 모두는 감염 질환의 예방 및 확산을 방지하기 위해서 희망을 가지고 일상 생활에서 기본 수칙을 준수하는 각 구성원이 되어야 할 것이다.
참고문헌
1. https://ko.wikipedia.org/wiki/바이러스
2. Coronavirus disease (COVID-19) Weekly Epidemiological Update and Weekly Operational Update, http://www.who.int
3. COVID-19 diagnostics in context, 3 June 2020, Sci. Transl. Med. 12, eabc1931 (2020)
4. https://www.360dx.com/coronavirus-test-tracker-launched-covid-19-tests
5. Molecular and Immunological Diagnostic Tests of COVID-19: Current Status and Challenges, iScience 23, 101406, August 21,
6. https://blog.addgene.org/sars-cov-2-covid-19-detection-methods-based-on-crispr-cas
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update