| 바이오마커를 단번에 검출할 수 있는 항체 센서 | |
|---|---|
| Date 2019-04-09 13:39:44 |
|

교수 / 학부생
홍익대학교 바이오화학공학과
heejinjeong@hongik.ac.kr / 4341ngu@naver.com
1. 항체를 이용한 면역측정법
항체는 동물의 체내에 바이러스, 미생물독소와 같은 외래물질(항원)이 침입하였을 경우 생산되는 당단백질이며, 항원을 포획하여 불활성화 시키거나 체외로 배출시키는 등 생체방어메커니즘에 있어서 중요한 역할을 한다. 항원에 대하여 높은 결합력과 특이성을 갖는 항체를 이용하여 샘플 안에 존재하는 항원을 고감도로 검출, 정량하는 면역측정법은 생물학의 기반연구에서부터 오염물질, 유해물질의 검사 및 병원물질의 진단, 치료까지 폭넓게 이용되고 있으며 그 중요성은 점점 증가하고 있다.
항원-항체 사이의 결합을 사용하여 항원을 검출하는 면역측정법중에서 일반적으로 널리 사용되는 방법인 enzyme-linked immunosorbent assay(ELISA)는, radioimmunoassay(RIA)와는 달리 방사성물질을 사용하지 않기 때문에 안전하며, 항원에 반응하는 1차항체, 그리고 그 1차항체에 반응하는 2차항체를 첨가한 후 최종적으로 효소반응에 바탕을 두는 발색반응을 이용하여 시그널을 얻어내기 때문에 감도 및 정량성이 좋은 점을 특징으로 들 수 있다. 하지만 ELISA로 대표되는 종래의 면역측정법은 항체 및 항원을 플레이트에 고정하는 과정, 플레이트상의 비특이적 반응을 억제하기 위한 블로킹 과정, 1차 및 2차 항체 반응 후의 비특이적인 흡착을 제거하기 위한 수차례의 세척과정을 필요로 하여 전체적으로 수시간의 시간이 소요되며 복잡한 과정을 필요로 하여 측정결과의 불균일을 초래하는 원인이 된다. 또한 1차항체 및 2차 항체의 ‘적절한’ pair선별이 요구된다. 때문에 고정화 및 세정과정을 필요로 하지 않는 호모지니어스한 면역측정법의 개발이 필요하다. 그자리에서(in situ) 간편하고 신속하게 항원을 검출 가능한 방법이 확립된다면, 특수한 장치 및 기술을 확보하는 필요가 없고 단시간에 실시결과가 얻어져서 임상검사를 포함한 다양한 분야의 현장수요에 부응가능하다.
현재까지 보고되어있는 호모지니어스 면역측정법의 한 가지로, 서로 다른 형광색소로 표지한 항체 또는 항체단편이 항원과 상호작용하는 것에 의해 형광색소사이의 형광공명에너지이동 (Förster resonance energy transfer, FRET)이 발생하는 원리를 이용하는 방법이 있다. 하지만 FRET를 이용한 면역측정법에서 시그널/백그라운드 비를 높이기 위해서는 형광색소간의 거리를 정교하게 조절해야 하며 특정거리 이상으로 두 가지 색소가 떨어져 있을 경우에는 전자이동효과를 기대하기 어려운 문제점이 있다. 또다른 호모지니어스 면역측정법의 예로, 항체의 말단에 녹색형광단백질(GFP)을 연결하여 형광면역측정에 이용하는 방법에 관한 연구가 보고되어 있지만, GFP의 크기가 크기 때문에 GFP를 융합하는 것에 의해 원래항체의 구조 및 기능에 영향을 미치는 경우가 있다. 본고에서는 상기한 기존의 면역측정법의 문제점을 획기적으로 해결할 수 있는, 고정화와 세척과정을 필요로 하지 않고 목적물질의 정량이 가능한 지금까지 없었던 unique한 형광측정원리를 기본으로 한 면역측정소자 Quenchbody에 대해 기술하기로 한다.
2. 항체 및 항체단편
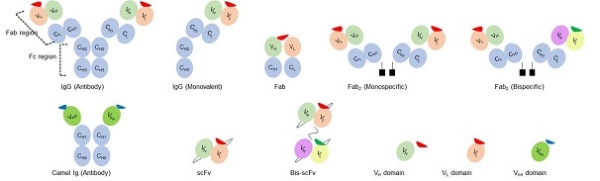
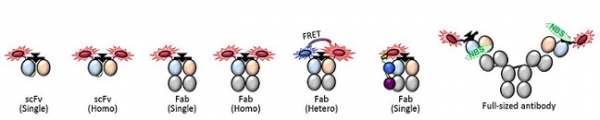
항원과 결합하여 면역반응을 일으키는 항체의 형태는 다양하게 존재하고 현재도 계속 개발되어지고 있다(그림 1). 사람, 쥐, 토끼, 염소 등에서부터 얻을 수 있는 IgG(Immunoglobulin)은 Y자형태로 heavy chain(중사슬)과 light chain(경사슬)으로 구성 되어있다. 특이하게 낙타과 알파카에서 얻을 수 있는 항체는 heavy chain으로만 이루어진 형태를 나타낸다. 항원결합부위를 포함하는 variable region(가변영역)과 그 외의 부분인 constant region(일정영역)으로 구분할 수 있는데, 이때 가변영역만 존재해도 항원을 인식할 수 있기 때문에 절단 또는 유전자재조합을 통해 가변영역 단독 또는 일정영역과의 다양한 조합의 항체단편을 생산할 수 있다.
그림 1. 항체 및 재조합항체단편의 구조
IgG의 Y자 형태에서 대칭구조의 절반인 형태를 monovalent라고 한다. 여기서 Fc부분을 제외한 나머지 부분을 fragment of antibody(Fab)라 하고 가변영역과 일정영역의 일부분을 포함하고 있는 형태이다. 가변영역은 항원결합 부위를 포함하면서 그 크기가 IgG보다 작기 때문에 고도로 밀집되어 있는 세포 사이 등 IgG가 침투하기 어려운 곳까지 침투할 수 있는 등의 장점을 갖는다. 또한 Fab2 (monospecific) 와 Fab’2 (bispecific)은 둘다 가변영역이 양쪽에 존재하지만 후자는 좌우에 다른 항원인식부위를 가지고 있다. 반면에 일정영역을 포함하지 않고 가변영역만 존재하는 항체단편도 있다. Single chain fragment of variable region(scFv)은 VH도메인과 VL도메인을 peptide linker로 연결한 형태이기 때문에 상기한 항체 및 항체단편 보다 크기가 작아 타겟 항원에 더 쉽게 접근할 수 있다. 마지막으로 VH, VL 단독의 경우, scFv, Fab, IgG 보다 항원결합부분이 적다는 단점이 있지만 크기가 작아 작은 공간사이를 침투하기 용이하기 때문에 세포 침투반응을 바탕으로 하는 면역반응을 성공시킬 수 있는 장점이 있다.
3. 항원과 결합하였을 때만 빛을 내는 형광항체단편 ‘Quenchbody’
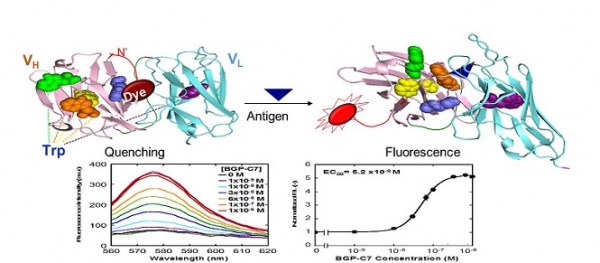
2012년 동경대학교 Ueda그룹에서는 부위특이적으로 형광색소를 도입한 항체단편이 항원이 존재하지 않을 경우에는 항체분자내의 tryptophan(Trp)에 의해 색소의 형광이 소광(quench)된 상태이지만, 항원 첨가 후에는 항체단편의 공간적 움직임이 발생하기 때문에 소광이 해소되어 형광을 발하는 원리를 발견하였고 이러한 원리에 의해 센서로 응용 가능한 형광항체단편을 Quenchbody라 명명하였다(그림 2) [1].
그림 2. Quenchbody의 작동원리 및 BGP검량선
Ueda그룹에서는 이러한 현상을 FRET을 이용한 open sandwich ELISA의 감도향상을 목적으로 한 실험과정에서 우연히 밝혀내었다. 구체적으로는 TAMRA(적색 색소), R110(녹색색소)로 표지한 항체의 VH와 VL를 1:1로 혼합한 후, 항원 첨가 후의 용액의 형광강도를 측정하였다. 그 결과, 항원 농도 의존적으로 형광이 증가함을 알수 있었고 FRET를 이용한 호모지니어스 면역측정과 관련한 본래의 실험목적을 달성하였다. 그런데 이 때 예상 외의 현상에 착목하게 되었는데, TAMRA표지 VH와 R110표지 VL를 동일한 몰수로 혼합하였음에도 불구하고 R110형광의 감소분보다 TAMRA형광의 증가분이 많다는 점이었다. 이를 확실히 하고자, 대조실험으로 VH만을 TAMRA로 표지하고 VL은 표지하지 않은 후 이들을 동일 몰수로 항원과 혼합한 결과, 항원 농도 의존적으로 형광강도가 증가한 것이었다. 형광강도변화가 항원의존성을 나타내기 때문에 이 원리를 이용함으로써 항원정량이 가능하며, 두 가지 형광색소를 이용해야 할 뿐만 아니라 두 색소사이의 거리를 정밀하게 조절하여야 하는 기존의 FRET방법과는 달리 본 원리를 이용하면 한 가지 색소만 사용하여도 형광응답을 얻을 수 있기 때문에 그 사용 가능성을 비약적으로 높일 수 있다고 생각하였다. 이후 본 형광색소표지항체단편을 Quenchbody로 명명하고 작용 메커니즘 및 응용범위의 범용화 등을 포함하여 보다 상세한 검토를 행하였다.
4. 왜 항원이 존재할 경우에만 빛을 내는가
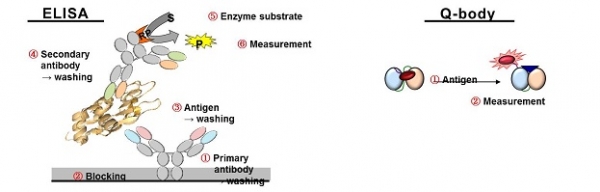
기존의 방법으로 형광색소를 표지한 항체는, 항원이 항체에 결합하기 전에도 빛을 내고, 항원이 결합을 해도 빛을 낸다. 따라서 항원 이외의 물질에 항체가 비특이적으로 결합한 경우와 항원에 항체가 결합한 경우의 형광시그널을 구분할 수 없기 때문에 항체를 첨가한 이후 정교하게 세척을 하지 않으면 background시그널이 높아진다. 이에 반해 Quenchbody는 항원 이외의 물질에 비특이적으로 결합한 경우에는 빛을 내지 않고 항원과 결합한 경우에만 빛을 내기 때문에 항체 첨가후 별도의 세척과정을 거치지 않고도 항원특이적 시그널을 얻을 수 있다(그림 3).
그림 3. 종래의 면역측정법과 비교되는 Quenchbody의 장점: Simple and Rapid
이러한 Quenchbody의 작동원리를 뒷받침하는 실험결과는 다음과 같다. 지금까지 Trp에 의해 형광색소가 소광하는 현상은 다방면에서 보고되어 있었고, 이는 Trp에서 색소로 광유기전자전이(Photoinduced Electron Transfer, PeT)가 발생하기 때문인 것으로 알려져 있다. Ueda 그룹은 실험적으로 우연히 발견한 Quenchbody의 작동원리가 Trp과 색소 사이의 PeT에 유래하는 것인지를 검증하기 위해, 골다공증 등의 바이오마커인 bone gla protein(BGP)을 인식하는 항체 내부의 Trp(VH을 이루는 아미노산 배열중의 33, 36, 47, 103번째, VL의 35번째의 아미노산이 Trp에 해당)을 각각 구조가 Trp와 유사한 아미노산인 Phe로 치환한 후 항원(BGP)존재하의 Quenchbody의 형광강도를 측정하였다. 그 결과 그 어느 변이체도 야생형(Trp에 변이를 도입하지 않은 경우)보다 항원 첨가 시의 형광강도의 증가 정도가 감소하였다(그림 4) [1]. 이를 통하여 항체에 존재하는 다섯 개의 Trp 이 모두 형광소광에 관여하고 있으며, 이들이 상호적으로 작용함으로써 색소가 소광됨을 알 수 있었다. 즉, 항체내부의 항원결합부위 근처에 존재하는 형광색소와 그 주변에 존재하는 Trp과의 전자이동에 의해 색소의 형광이 소거되어 있었으며, 그 후 항원을 첨가하면 항체가 항원과 결합을 하면서 분자운동이 일어나기 때문에 항체내부에 위치한 색소와 Trp과의 상호작용이 약해져서 소광이 해소되는 가능성을 시사하였다. 이러한 가능성은 이후의 실험(브라운운동을 바탕으로 한 편광실험[2], 3D 입체구조를 바탕으로 한 색소-Trp위치 해석[3])에서 더욱 뒷받침 되었다. 이외에도 항원첨가에 의해 소광이 해소되는 원리의 힌트가 된 실험결과는, Quenchbody용액에 항원 대신 단백질변성제(Guanidine HCl + DTT)를 첨가한 경우에 항원을 첨가한 경우와 비슷한 정도로 형광강도가 증가한 것이다. 즉, 변성제를 첨가함으로써 단백질의 고차구조가 파괴되어 색소와 Trp과의 공간적 거리가 증가하여 Trp의 전자이동에 의한 소광이 해소되는데, 항원이 첨가되었을 때 scFv의 VH와 VL이 공간적으로 이동하여 변성제를 첨가하였을 때와 유사한 현상이 일어났을 가능성이 있다[1-13].
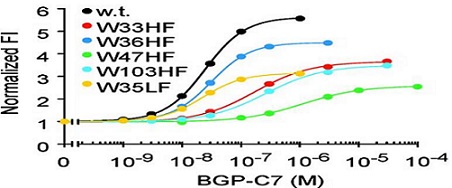
그림 4. Quenchbody의 quencing현상은 항체내부의 Trp (W)가 관여한다. [1]에서 발췌.
5. 무세포전사번역계를 이용한 Quenchbody 작성
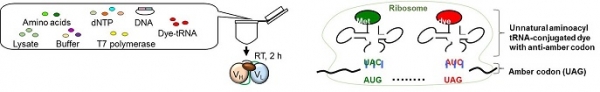
개발초기의 Quenchbody는 무세포 단백질 전사 번역계와 부위 특이적 비천연아미노산 도입기술을 이용하여 작성되었다[1-5]. ScFv배열의 N말단부근에 형광색소결합배열(amber codon, UAG)을 도입한 DNA와, 단백질의 전사번역에 필요한 효소, 아미노산, 라이세이트 등을 혼합함으로써 세포 내의 단백질합성인자를 시험관 내에서 재구성하여 단백질을 합성하는데, 이때 반응계에 anti-amber codon(CUA)이 연결된 형광색소 표지 tRNA를 혼합함으로써 부위특이적으로 형광색소를 도입한다. 이러한 방법을 이용하였을 경우 약 2시간 내에 Quenchbody를 합성하는 것이 가능하였다(그림 5). 이러한 방법으로 BGP이외에도 세포골격을 구성하는 단백질인 비멘틴의 인산화, 위법마약 등을 검출하기 위한 Quenchbodies를 작성하는 데에 성공하였고, TAMRA(적색) 이외에도 R6G (오렌지색), ATTO520 (녹색) 등의 다양한 색소를 항체에 표지가능하였으며 색소별로 상이한 형광응답을 나타내는 것에 대한 지견을 얻을 수 있었다.
그림 5. 무세포 전사번역계를 이용한 Quenchbody구축
6. 다양한 형태의 항체단편을 이용한 Quenchbody
여기서 scFv보다 천연항체 구조에 가까우며 링커 없이도 구조적으로 안정한 Fab단편을 이용하여 Quenchbody를 작성한다면 보다 새로운 지견을 얻을 수 있다고 생각하여 무세포전사번역계를 이용하여 BGP를 인식하는 Fab단편을 발현시키고 H chain의 N말단을 형광색소로 표지한 Quenchbody를 작성하였다. 그 결과 scFv 형태의 Quenchbody(6배)보다 높은 10배의 형광응답이 얻어졌다[5]. ScFv를 이용한 경우 VH와 VL을 인공적인 펩타이드링커로 연결시키기 때문에 VH와VL사이의 상호작용을 증가시키는 것이 가능하지만 인공적인 링커를 부가함으로서 항체가 본래 갖고 있는 항원과의 결합활성 등의 기능이 저하될 수 있다. 반면에 VH와 CH로 구성되는 poly peptide와 VL과 CL로 이루어지는 poly peptide가 disulfide결합에 의해 hetero dimer protein을 구성하는 Fab라면 항체가 갖는 본래의 기능을 유지하고 항원 비존재 시에는 형광색소가 보다 소거되어 background 시그널을 저하시켜서 결과적으로 보다 높은 형광응답을 나타내었다고 생각되었다.
더 나아가서 Fab의 H chain 또는 L chain 중의 한쪽의 N말단을 형광표지한 경우에 비해 양쪽의 N말단을 같은 색의 색소로 double labeling한 경우 항원 존재 시 최대 26배까지 형광증가를 나타내어, 형광색소와 Trp사이의 PeT원리를 바탕으로 한 형광 소거에 덧붙여 색소끼리의 근접에 의한 소거 효과가 추가되었음을 알 수 있었다. 또한 H chain과 L chain의 양쪽을 다른 색의 형광색소로 표지한 경우 약 50배의 형광강도를 증가시킴에 성공하였으며, 서로 다른 색소 사이의 FRET효과가 부가되었다고 예상되었다. 이외에도 응답을 향상시키기 위해 Quenchbody에 도입하는 형광색소의 수 및 Quenchbody의 기본골격이 되는 항체단편에 대한 연구가 활발히 이루어지고 있다(그림 6).
그림 6. 목적에 맞게 항체단편의 형태 및 색소의 종류 등을 ‘디자인’하여 Quenchbody를 작성 가능하다.
7. 대장균을 이용한 Quenchbody 대량생산
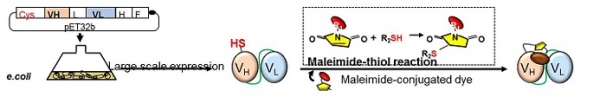
상기한 무세포전사번역계를 이용할 경우 짧은 시간 안에 Quenchbody의 구축이 가능하지만 무세포전사번역계 시약이 고가이기 때문에 세포 이미징 및 in vivo 실험 등 센서를 대량으로 필요로 하는 경우 Quenchbody의 작성에 한계가 있었다. 이를 극복하기 위해 대장균을 이용하여 항체를 대량으로 합성하고anti-amber codon tRNA와 결합된 특수한 색소보다 저렴한 maleimide 결합 색소를 사용하여 Quenchbody를 작성하고자 시도하였다. 구체적으로는 BGP인식 항체의 Fab단편을 대장균에서 발현, 정제한 후 H chain 및 L chain의 말단에 부가한 Cysteine 에 maleimide부착색소를 maleimide-thiol반응을 이용하여 표지하였다(그림 7). Fab이외에도 scFv형태의 Quenchbody의 경우에도 대장균을 이용하여 Quenchbody를 작성함에 성공하였고, 시판중인 다양한 색상의 maleimide부착 색소로 표지 가능함을 밝혔다[6-12].
그림 7. 대장균을 이용한 Quenchbody의 대량생산
8. 세포이미징에의 응용
Quenhbody을 이용한 세포 이미징 또한 가능하다. 인간뼈 육종세포 U2OS를 배양한 후, U2OS의 분화를 촉진하고 BGP생산을 유도하는 비타민D3를 첨가하여 반응시킨 후 Quenchbody를 첨가하여 형광현미경 관찰을 하였다. 비교를 위해 비멘틴D3 또는 Quenchbody를 첨가하지 않은 조건을 동시에 수행하였다. 그 결과 비타민D3로 세포의 전처리를 행하고 Quenchbody를 첨가하였을 경우에만 세포의 형광이 관찰되었고, 이 결과를 통하여 Quechbody를 이용하여 BGP를 생산하는 골아세포의 이미징에 성공하였으며 Quenchbody를 간편하고 신속한 형광 이미징 센서로 사용 가능함을 알 수 있었다[5]. 또한 암세포의 바이오마커인 Claudin을 인식하는 Quenchbody를 이용한 암세포 이미징[9] (그림8), 유방암 관련 HER2 이미징 [in preparation]에도 성공하였다. Quenchbody를 이용한 세포 이미징의 우수한 특징으로, Quenchbody를 첨가한 후에 세척과정이 필요하지 않고 첨가 후 바로 그 형광을 관측할 수 있기 때문에 세척이 불가능한 세포 내(소포체 등)의 관찰이 가능한점, 반응시간이 수초에서 수분 정도로 매우 짧기 때문에 시간별로 실시간 이미징이 가능한 점을 들 수 있다.
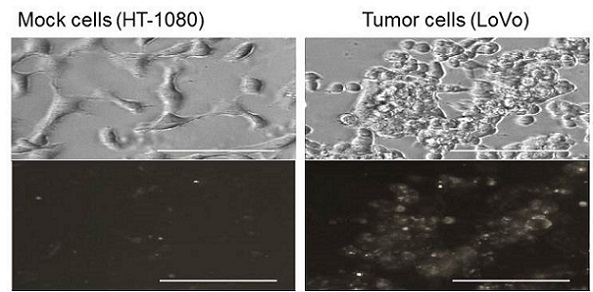
그림 8. Quenchbody를 이용한 암세포 이미징. [9]에서 발췌
9. 간편신속한 항체센서로서의 범용성 증대
BGP 항체의scFv중의 5개의 Trp중의 4개가 BGP 항체 이외의 항체의 가변영역 내부에 존재하는 확률을 항체배열 데이터베이스에서 조사하면 그 보존성은 94% 이상으로, 이는 원하는 항체를 이용하여 Quenchbody를 작성할 수 있음을 시사한다. 현재까지 Quenchbody의 작성 예로는 여성호르몬 에스타지올 [in preparation], 내분비산란작용에 관련하는 비스페놀A[1]과 같은 저분자에서부터 닭난백리조자임[3]및 혈청알부민[13] 등과 같은 고분자단백질까지 항원 크기에 상관없이 수십개 종류의 다양한 항원 검출 성과를 보이고 있다. 또한 이러한 형광소거의 원리는 항원항체반응 이외에도 단백질 상호작용 검출센서에도 응용되고 있다.
Quenchbody를 이용한 면역측정은, 블로킹 및 세척과정뿐만이 아니라 1차, 2차, 3차항원과 같은 연속적인 항체의 사용이 불필요하기 때문에 ‘항원과 Quenchbody를 섞는 것 만으로’ 간편하고 신속하게 그자리에서 목적항원을 검출 가능하다는 최대 이점을 갖는다. 이러한 Quenchbody를 의료 및 약제 연구 및 식품안정성 평가, 환경분석, 약물측정 등의 다양한 범위의 목적항원 검출이 가능하고, 특히 어려운 전문기술이 없어도 쉽게, 그리고 저가로 손쉽게 구입하여 사용할 수 있는 on site검출계로 전개됨이 기대된다.
참고문헌
1. Ryoji Abe et al., “Quenchbodies”: Quench-Based Antibody Probes That Show Antigen-Dependent Fluorescence. JACS, 2012.
2. Hiroyuki Ohashi et al., Insight into the working mechanism of Quenchbody: transition of the dye around antibody variable regions that fluoresces upon antigen binding. Bioconj Chem. 2016.
3. Hee-Jin Jeong and Hiroshi Ueda. Strategy for making a superior Quenchbody to proteins: effect of the position of fluorophore. Sensors, 2014.
4. Hee-Jin Jeong et al., Detection of vimentin serine phosphorylation by multicolor Quenchbodies. Biosens Bioectron, 2013.
5. Ryoji Abe et al., Ultra Q-bodies: quench-based antibody probes that utilize dye-dye interactions with enhanced antigendependent fluorescence. Sci Rep. 2014.
6. Hee-Jin Jeong et al., A signal-on fluorosensor based on quench-release principle for sensitive detection of antibiotic rapamycin. Biosensor. 2015.
7. Hee-Jin Jeong et al., Q-bodies from recombinant single chain Fv fragment with better yield and expanded palette of fluorophores. ACS Sens. 2016.
8. Hee-Jin Jeong et al., One-pot construction of Quenchbodies using antibody binding proteins. Anal Methods, 2016.
9. Hee-Jin Jeong et al., Development of a Quenchbody for the detection and imaging of the cancer-related tight-junction associated membrane protein claudin. Anal Chem. 2017.
10. Shitao Zao et al., Rapid detection of the neonicotinoid insecticide imidacloprid using a Quenchbody assay. Anal Bioanal Chem. 2018.
11. Ako Sasao et al., Development of a fluvoxamine detection system using a Quenchbody, a novel fluorescent biosensor. Drug Testing and Analysis. 2018.
12. Hee-Jin Jeong et al., Single-step detection of influenza virus hemagglutinin using bacterially produced Quenchbodies. Sensors. 2018.
13. Hee-Jin Jeong et al., Construction of dye stapled Quenchbody by photochemical crosslinking to antibody nucleotide-binding site. Chem Comm. 2017.
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update