| 경북대학교 나노바이오공학 연구실 NABI Lab (Nano Bio-engineering Lab) | |
|---|---|
| Date 2020-10-21 03:58:06 |
|

경북대학교 나노바이오공학 연구실 NABI Lab (Nano Bio-engineering Lab)
1. 여는 말
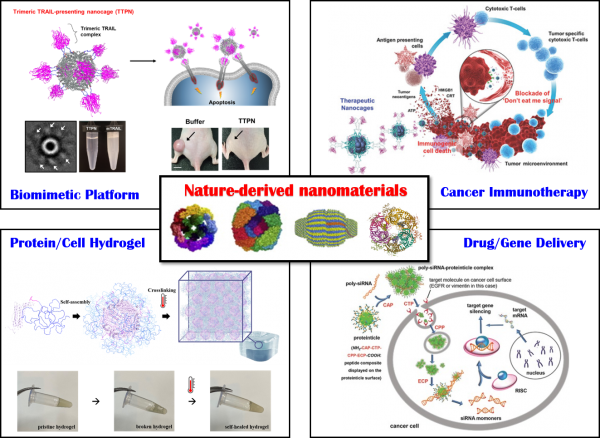
경북대학교 나노바이오공학 연구실, NABI Lab (Nano Bio-engineering Lab) 을 소개합니다. 저희 연구실은 이은정 교수님 (화학공학과) 지도 아래 석사과정 3명, 학부 연구생 2명의 연구원이 있습니다. 저희는 나노바이오의 여러 분야 중 에서도 기능성과 안전 ·안정성을 갖춘 나노바이오물질을 연구하고 있으며, 특히 “자연 유래 나노소재의 개발 및 응용 ”에 집중하고 있습니다. 이러한 나노바이오소재는 bio assay, in vivo & in vitro diagnostics, drug delivery system, biocatalyst, material science 등 다양한 분야에 적용할 수 있으며, 현재는 천연단백질을 활용한 생체적합성 소재 개발 기초 연구에서부터 면역항암치료 응용 연구까지 폭넓은 연구 활동을 하고 있습니다.
2. 연구실 분위기
저희 연구실은 2017년 3월에 신설된 신생연구실로, 교수님을 포함한 연구실 평균 연령이 비교적 낮기 때문에 “수평적인 분위기 ”를 가지고 있습니다. 그 덕분에 서로 대화가 많은 편이고 전반적으로 생동감이 넘칩니다. 연구원들 간에 부담 없이 자유로운 소통을 할 수 있으며, 그 과정에서 원활한 의견공유가 이루어져 더욱 창의적인 연구 아이디어를 얻을 수 있습니다. 또한 정기적인 미팅을 통해 연구원들 간 서로의 연구에 대해 깊이 있게 이해하며, 더 나아가 적극적으로 질문하고 연구 과정을 공유하고 있습니다. 이러한 원활한 소통 덕분에 각자 다른 주제의 연구를 진행하면서도 다른 연구원들의 연구로부터 모든 구성원들이 배우며 발전할 수 있습니다. 또한, 실험적인 부분에 있어서도 각자의 실험 노하우가 잘 공유되고, 실험실 업무 분담도 잘 되어 있어 연구활동에 전념하기 수월합니다.
3. 특징
저희 연구실의 특징은 다른 학문분야와의 활발한 연계를 통해 다양한 연구 관점 및 범위를 넓히는 데 적극적이라는 것을 들고 싶습니다. 현재, InterMembrane Signaling 연구실 (한국과학기술연구원), 분자생물공학 연구실 (고려대학교),기능성미생물생리학 연구실 (충북대학교)을 비롯하여, 학내에서는 나노포토닉스응용전자 연구실 (전자공학부), 기능성 나노소재 연구실 (응용화학과) 및 미생물대사공학 연구실 (식품응용공학과) 등 다양한 학문의 연구팀과 밀접한 협업 연구를 진행하고 있습니다. 다양한 학문 분야의 연구자들과의 연계는 저희 연구실의 연구과제 진행 및 해결 방향에 대해 다른 관점에서 새로운 아이디어를 제공해 줄 수 있으며, 이러한 융합 연구를 통해 보다 혁신적인 기술을 개발하고자 노력하고 있습니다.
4. 연구
저희가 주로 연구하는 분야는 나노메디신 (nano-medicine) 분야입니다. 나노메디신 분야는 질병의 치료, 진단 및 예방을 위한 목적으로 나노기술을 이용하여 분자수준에서 설계 및 제조하는 기술로서, 기존 의료기술의 한계를 극복할 수 있는 신개념 치료, 분석기술입니다. 실제로 저희는 단백질로 이루어진 나노입자를 비롯한 다양한 자연 유래의 나노소재를 발굴 ·개발하고, 이를 나노메디신 분야에 적용하는 연구를 진행하고 있습니다. 저희 연구실의 다양한 연구 테마 중에서 현재 진행 중인 프로젝트 4가지만 간략히 소개드리겠습니다.
첫 번째로, 항암면역치료의 기초 연구가 되는 신물질을 개발하고 있습니다. 면역항암요법은 인체의 면역체계를 이용해서 암을 치료하는 방법으로, 부작용과 약물 저항성을 획기적으로 줄일 수 있는 치료방법입니다. 저희 연구실에서는 대표적으로 세포자살유도 단백질과 면역관문억제 단백질을 이용한 새로운 면역항암치료제재를 연구하고 있습니다. 특히, 생체 내 존재하는 면역항암 단백질의 구조를 모방하여 기존 대비 치료 효율을 극대화시킬 수 있는 신 치료물질 및 기술을 개발하고 있습니다.
두 번째로, ‘Plug-In Platform’을 개발하고 있습니다. 즉, 기 개발된 나노소재에 기능성 물질을 부착할 때 더 쉽고 빠르게 기능성을 부여할 수 있는 플랫폼을 제작하는 것입니다. 저희가 개발 중인 이 나노 플랫폼은 DNA를 조작할 필요 없이 이미 만들어져 있는 단백질을 plug-in 방식으로 표면에 부착 가능하기 때문에, 재조합 단백질 합성 시간을 줄일 수 있을 뿐 아니라 하나의 나노소재에 여러 종류의 bio-functionality를 부여할 수 있다는 장점이 있습니다.
세 번째로, 저희는 기존 고분자 소재 대비 하이드로젤의 생체 적합성을 높이기 위하여 단백질 기반의 인체 친화적인 하이드로젤을 개발하는 연구를 진행 중입니다. 특히 저희는 protein, cell, microvesicle 기반 하이드로젤을 제작하는 등 하이드로젤의 다각화에 주력하고 있습니다. 하이드로젤의 다각화는 하이드로젤 기반 tissue engineering 및 3-D 프린팅 기술로의 개발 및 응용의 폭을 넓혀줄 것으로 기대하고 있습니다.
마지막으로 위 기초 연구들의 빠른 산업화를 위하여 기 개발된 소재의 안전 ·안정화 향상 기술을 개발 중입니다. 자연 유래의 소재는 생체적합성이 뛰어나 활용 범위가 넓지만 체내 반감기가 짧다는 특유의 성질 때문에 인체 내에서 안정성이 부족합니다. 이러한 성질로 인해 자연 유래 소재 기반 의약품이 약효를 내기도 전에 몸 안에서 분해되어 사라져버리는 등 상업화를 하는 데 어려움을 겪는 경우가 있습니다. 저희 연구실에서는 이러한 단점을 극복하고자, 인체 내에서 안정성을 높일 수 있는 기술을 개발하고 있습니다. 이는 자연 유래의 소재의 산업화를 촉진하는 기반 기술이 될 것으로 생각됩니다.
5. 맺음말
저희 나비랩 [NABI Lab (Nano Bio-engineering Lab)]은 자연 유래의 바이오소재를 분자 수준에서 설계 및 가공하여 이를 체내 ·체외 진단, 치료, 백신, 나노촉매, 재료과학 등과 같은 다양한 분야로의 응용 기술 개발을 목표로 하고 있습니다. 또한, 금속, 고분자, 줄기세포, 엑소좀 등 다양한 유 ·무기 물질과의 융복합 연구 등을 통해 기존 연구의 적용 범위 및 실용화 측면에서 확대하고자 연구에 매진하고 있습니다. 저희 연구실에서는 모든 구성원이 각자의 위치에서 연구에 충실히 매진하여 끊임없이 도전하고 있으며, 국내·외 생물공학 발전에 크게 기여할 수 있는 세계적 수준의 연구실로 거듭나기 위해 아낌없는 노력을 기울이고자 합니다.
6. 연구실 대표 논문
1. H. Je, G.H. Nam, G.B. Kim, W.Kim, S.R. Kim, I.-S. Kim* & E.J. Lee*, Overcoming therapeutic efficiency limitations against TRAIL-resistant tumor using re-sensitizing agent-loaded trimeric TRAIL-presenting nanocages, Journal of Controlled Release, Under review (2020)
2. W. Ahn, W. Kim, H.M. Lee, I.W. Cheong & E.J. Lee*, Structurally Hierarchical Self-Healing Protein Hydrogel Made of Nanocage Crystals Conjugated with Intrinsically Disordered Proteins. Biomaterials, Under review (2020)
3. M. Kih§, E.J. Lee§, N.K. Lee, Y.K. Kim, K.E. Lee, C. Jeong, Y. Yang, D-H. Kim, & I.-S. Kim*, Designed trimermimetic TNF superfamily ligands on self-assembling nanocages. Biomaterials 180, 67-77 (2018) (§ equally contributed)
4. G.H. Nam§, E.J. Lee§, Y.K. Kim, Y. Hong, Y. Choi, M.J. Ryu, J. Woo, Y. Cho, D.J. Ahn, Y. Yang, I.C. Kwon, S.Y. Park* & I.-S. Kim*. Combined Rho-kinase inhibition and immunogenic cell death triggers and propagates immunity against cancer. Nature Communications 9, 2165 (2018). (§ equally contributed)
5. E.J. Lee§, G.H. Nam§, N.K. Lee, M. Kih, E. Koh, Y.K. Kim, Y. Hong, S. Kim, S.Y. Park, C. Jeong, Y. Yang, & I.-S. Kim*. Nanocage-Therapeutics Prevailing Phagocytosis and Immunogenic Cell Death Awakens Immunity against Cancer. Advanced Materials 30, 1705581 (2018). (§ equally contributed)
6. N.K. Lee§, E.J. Lee§, S. Kim, G.H. Nam, M. Kih, Y. Hong, C. Jeong, Y. Yang, Y. Byun, & I.-S. Kim*. Ferritin nanocage with intrinsically disordered proteins and affibody: A platform for tumor targeting with extended pharmacokinetics. Journal of Controlled Release. 267, 172 (2017). (§ equally contributed)
7. E.J. Lee, N.K. Lee, & I.-S. Kim*. Bioengineered protein-based nanocage for drug delivery. Advanced Drug Delivery Reviews. 106, 157 (2016).
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update